خصائص الفلزات واللافلزات ، تم تقسيم العناصر الكيميائية إلى عدة أنواع طبقاً لخواصها ونشاطها الكيميائي، ومن أهم تصنيفات العناصر هي العناصر الفلزية واللافلزية، وعلى موقع قلمي من خلال قسم الكيمياء سوف نتعرف على أهم خصائص الفلزات واللافلزات
العناصر الكيميائية
العناصر الكيميائية هي المواد التي تتكون من ذرة واحدة، وما يميز كل عنصر عن الآخر هو اختلاف العدد الذري لكل منهم والذي يمثل عدد الإلكترونات أو عدد البروتونات الخاصة بذرة العنصر.
ولكل عنصر اسم خاص به ورمز كيميائي مختلف يمثل أول حرف من اسم العنصر باللغة اللاتينية، وفي حالة تشابه أول حرف بين عنصرين يتم استخدام أول حرفين.
وتوجد العناصر الكيميائية في الطبيعة إما في أجساد الكائنات الحية بمختلف أنواعها أو في البحار والجبال والمجرات والنجوم، وبعض العناصر لا يمكن الحصول عليها إلا من خلال تحضيرها في مختبر الكيمياء، وقد تكون العناصر ثابتة ومستقرة ولا تتغير أو تكون غير مستقرة.
خصائص الفلزات واللافلزات
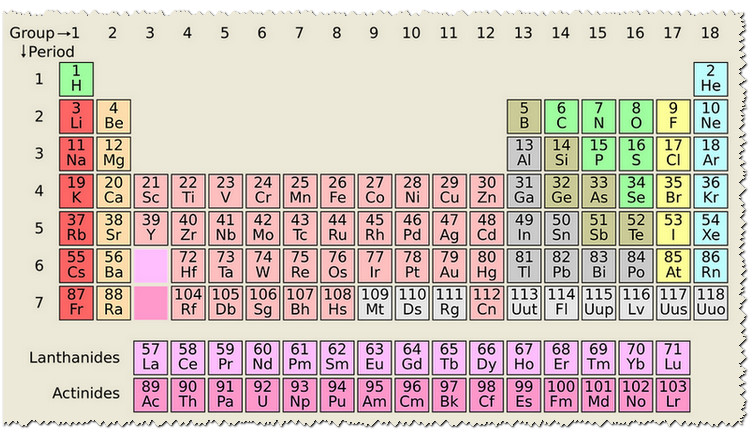
وتم تقسيم العناصر في الجدول الدوري إلى العناصر الفلزية وأشباه الفلزات والعناصر اللافلزية والسطور التالية توضح خصائص الفلزات واللافلزات
الفلزات Metals
هي العناصر التي تفقد إلكترونات التكافؤ عند دخولها في التفاعل الكيميائي لتصل إلى حالة الاستقرار وتتحول إلى أيون موجب، وترتبط ذرات العناصر الفلزية بروابط فلزية، وتترتب أيوناتها في شكل شبكة.
وقد ظهر أنه عند تمرير خطاً مائلاً من عنصر البورون وحتى عنصر البولونيوم فسوف تنفصل الفلزات عن اللافلزات تلقائياً.
ومن أهم العناصر الفلزية المستخدمة في العديد من المجالات: النحاس، الذهب، الفضة، الألومنيوم، الرصاص، الحديد، ويمكن الحصول على هذه العناصر من الطبيعة.
تمثل العناصر الفلزية أكثر العناصر تواجداً في الجدول الدوري؛ حيث تُقسَّم إلى: الفلزات القلوية، الفلزات القلوية الترابية، الفلزات النبيلة، الفلزات الضعيفة، الفلزات الانتقالية، والسبائك.
خصائص الفلزات
- تمتاز الفلزات بارتفاع كثافتها.
- لها بريق ولمعان وتكون قابلة للطرق والسحب.
- موصل جيد للحرارة والكهرباء، ودرجة انصهارها مرتفعة.
- الفلزات من العناصر النشطة كيميائيا والغير مستقرة، وتتأكسد عند تعرضها للأكسجين لأنها تتفاعل بشكل سريع معه.
- يمكن تشكيل العناصر الفلزية بسهولة.
اللافلزات Non-metals
هي العناصر التي تكتسب إلكترون أو أكثر لتصل إلى حالة الاستقرار لأقرب غاز خامل وتتحول إلى أيون سالب، ويتم ذلك إما من خلال التفاعل مع العناصر الفلزية وتكوين روابط أيونية، أو من خلال التفاعل مع عناصر لا فلزية أخرى وتكوين روابط تساهمية، وتتركز العناصر الفلزية أعلى يسار الجدول الدوري باستثناء عنصر الهيدروجين الذي يوجد أعلي يمين الجدول مع الفلزات القلوية.
ومن أهم العناصر اللافلزية: الهيدروجين، الأكسجين، النيتروجين، الفسفور، الكلور، البروم، الكبريت، اليود.
خصائص اللافلزات
- لا يوجد لها بريق معدني ويكون لونها أسود داكن.
- لها حجم ذري صغير وسالبية كهربية مرتفعة.
- غير قابلة للطرق أو السحب ولا يمكن تشكيلها.
- لها درجة انصهار منخفضة، ورديئة في توصيل الحرارة والكهرباء.
- توجد العناصر اللافلزية في أكثر من حالة؛ فبعضها صلب مثل: الكبريت، واليود، وبعضها غاز مثل: الأكسجين، النيتروجين، الهيدروجين.
- بعض العناصر اللافلزية نشطة كيميائياً مثل: الكلور، الفلور، وبعضها خامل مثل: النيون، والهيليوم.
- عدد الإلكترونات في الغلاف الخارجي للعناصر اللافلزية (إلكترونات التكافؤ) يكون أكثر من 4.
- يمكن للعناصر اللافلزية أن تتفاعل مع عنصر الأكسجين مكونة الأكاسيد الحمضية، ولكنها لا تتفاعل مع الأحماض الخفيفة.
 قلمي قلمي موسوعة قلمي الشاملة.
قلمي قلمي موسوعة قلمي الشاملة.