عدد العناصر في الجدول الدوري ، دائما ما يسعى العلماء إلى ابتكار الطرق والخطوات التي تجعل الدراسة العلمية أكثر سهولة، ومن المعروف أن علم الكيمياء يقوم على دراسة خواص وسلوك العناصر الكيميائية، ولذلك فقد حرص علماء الكيمياء على الوصول إلى طريقة تسهل دراسة خواص هذه العناصر، وكثرت محاولاتهم إلى أن نجحوا في وضع الجدول الدوري للعناصر.
وعلى موقع قلمي سوف نتعرف على الجدول الدوري بالإضافة إلى عدد العناصر في الجدول الدوري والأسس التي تم الاعتماد عليها في ترتيب العناصر به.
الجدول الدوري
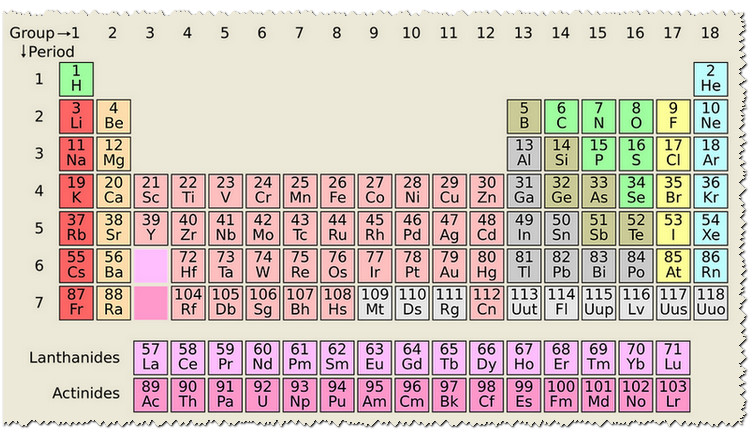
يتم تعريف الجدول الدوري للعناصر بأنه عبارة عن طريقة متطورة لترتيب كل العناصر الكيميائية المعروفة في جدول يتكون من 7 دورات أفقية و18 مجموعة رأسية، بالإضافة إلى سلسلة اللانثانيدات وسلسلة الأكتينيدات.
تأسيس الجدول الدوري
أول من قام بوضع تصور مبني على أساس صحيح للجدول الدوري هو عالم روسي يُدعى ديمتري مندليف عام 1869م، حيث قام بترتيب العناصر الكيميائية اعتماداً على الزيادة في الكتلة وكان يحتوي الجدول في هذا الوقت على 66 عنصر فقط.
وشهد الجدول عدد من التطورات إلى أن قام عالم آخر يُدعى هنري موزلي عام 1911م بترتيب العناصر في الجدول الدوري وفقاً للزيادة في العدد الذري، حيث أن العدد الذري هو عدد البروتونات الموجبة الموجودة داخل نواة العنصر أو عدد الإلكترونات السالبة التي تدور حولها.
عدد العناصر في الجدول الدوري
أصبح لا غنى عن استخدام الجدول الدوري للتعرف على خواص العناصر بسرعة وسهولة، وتنقسم مجموعات الجدول الدوري إلى 8 مجموعات رئيسية مع 10 مجموعات خاصة بالعناصر الانتقالية، والثمانية مجموعات الرئيسية هي:
- مجموعة المعادن القلوية (يحتوي المدار الخارجي بها على إلكترون واحد).
- مجموعة المعادن القلوية الترابية.
- مجموعة المعادن الضعيفة.
- مجموعة أشباه المعادن.
- مجموعة اللامعادن.
- مجموعة الهالوجينات.
- مجموعة الغازات النبيلة (يحتوي المدار الخارجي بها على 8 إلكترونات).
أما باقي مجموعات الجدول الدوري التي تتوسط الجدول فهي مجموعات العناصر الإنتقالية والتي تنقسم إلى عناصر انتقالية داخلية وعناصر انتقالية رئيسية.
ويحتوي الجدول الدوري للعناصر الآن على (118) عنصر، حيث تم إضافة 4 عناصر جديدة إليه عام 2016م وهي: (أنون بنتيون ورقمه (113)، أنون تريوم ورقمه (115)، أنون أوكتيوم ورقمه (117)، أنون سيبتيوم ورقمه (118)).
والعناصر الموجودة في الجدول الدوري من بداية الجدول وحتى العنصر رقم 98 موجودة بشكل طبيعي أما العناصر من 99 وحتى نهاية الجدول فلا يمكن الحصول عليها إلا من خلال التفاعلات والتجارب في مختبر الكيمياء.
وقد قام العلماء بإعطاء كل عنصر رمز كيميائي خاص به وهذا الرمز يمثل أول حرف أو أول حرفين من اسم العنصر باللغة اللاتينية.
خصائص الجدول الدوري
- في عناصر المجموعة الواحدة يكون عدد إلكترونات التكافؤ الموجودة في المدار الخارجي للذرة متساوي.
- تتشابه عناصر كل مجموعة في خواصها، ويزداد عدد إلكترونات التكافؤ عند الانتقال جهة اليمين بالجدول.
- في دورات الجدول الدوري يكون عدد مستويات الطاقة التي تحتلها إلكترونات ذرة العنصر متساوياً لكل عناصر الدورة الواحدة.
- العناصر المعدنية موجودة يسار الجدول وهي عناصر صلبة في درجة حرارة الغرفة باستثناء عنصر الزئبق، وتتميز هذه العناصر بالبريق وقدرتها على توصيل الكهرباء وقابليتها كذلك للطرق والسحب.
- أما العناصر اللامعدنية فهي موجودة يمين الجدول، ومن صفات هذه العناصر انخفاض درجة الانصهار وانخفاض قدرتها على توصيل الحرارة والكهرباء، وهي في درجة حرارة الغرفة تكون متنوعة ما بين الحالة الصلبة والسائلة والغازية.
 قلمي قلمي موسوعة قلمي الشاملة.
قلمي قلمي موسوعة قلمي الشاملة.